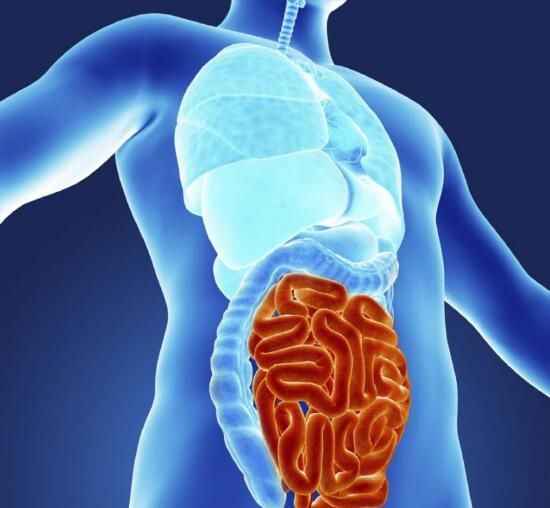
肠道微生物是生活在我们机体中的肠道菌群,这类特殊的微生物对机体营养物质代谢、机体发育、免疫力以及多种疾病的发生等方面都非常重要。
近些年来,很多科学家都发现肠道微生物与多种人类疾病发生存在着直接的关联,比如癌症、肥胖、心血管疾病等,此外,研究者还发现肠道菌群与神经变性疾病,比如阿尔兹海默式症、帕金森疾病等存在一定关联。
【1】Cell: 肠道微生物调节帕金森疾病的发病过程
doi:10.1016/j.cell.2016.11.018
最近一项研究似乎改变了我们长久以来对帕金森症发病的固有观念。
这项研究认为,帕金森症的病发并不是起始于大脑,而是与肠道微生物有关。这一观点能够解释为什么帕金森症患者会首先出现便秘的症状,十几年之后才会进而产生其它并发症。
帕金森症经常与颤动,肢体僵硬,运动不便等相关联,而主要原因是大脑内部的关键神经元发生了损伤。
尽管目前有一些能够针对神经退行性疾病的治疗手段,但并没有完全预防或治疗的效果,而且研究者们至今也不清楚该疾病的发生与恶化的分子机制。
【2】Nat Med:肠道微生物能够保护大脑免受中风的风险
原文阅读:Tweaking our gut bacteria could help protect our brain from strokes
最近的研究表明我们肠道内的微生物对我们的生理与心理健康具有重要的意义,影响着我们的胃口以及我们的思想。
如今,一项新的研究表明肠道微生物能够保护我们的大脑不受损伤。小鼠试验证明,一类特殊的肠道微生物的存在能够降低我们患中风的风险。
“我们的试验表明大脑与肠道存在一种新的联系”,来自康奈尔大学脑科学研究所的神经学家Josef Anrather说道:“这种肠道微生物能够调节中风的发病风险,这将改变医学界对于中风的一贯见解”。
Anrather等人设置了两组小鼠,一组利用抗生素处理,清除其肠道内的微生物,另一组作为对照。两星期以后,科学家们向两组小鼠同时进行了缺血性中风的诱导(即通过堵塞通向大脑的血管,致使脑部缺氧)。
【3】肠道微生物会影响帕金森?!
原文报道:Gut Bacteria May Influence Parkinson's Risk, Phenotype
来自芬兰的研究者们发表了一项新的研究成果:他们通过比较正常人与帕金森(PD)患者肠道微生物成分特征,发现相比于正常样本,PD患者肠道微生物群中普雷沃氏菌科的丰度发生了明显的下降。这一发现可能为研究PD的发生提供了一条非常有价值的线索。
“尽管这一发现仅仅是‘表面工作’(指研究部位较浅)”,然而却为我们深入研究提供了极佳的理由",芬兰赫尔辛基大学大学神经学系的教授,Filip Schepenjans博士说道。“如果进一步的研究能够证明PD是由于肠道这种特定微生物的缺失而引发的,那么向患者体内补充此种微生物就可能减缓疾病的恶化,甚至阻止疾病的发生。”
相关研究成果发表在《Movemont Disorders》杂志的三月刊上。
“这是一项非常有意思的发现”,Schepenjans说:“我们将会重点研究这一问题,因为我们研究这项课题的最终目的就是要找到那些我们能够改变的因素”。然而,一个更加迫切的目标就是要确认肠道微生物组成分的改变在PD出现前就已经发生。

【4】Sci Rep:肠道细菌或和多发性硬化症发病相关
doi:10.1038/srep28484
如果被问及有害的肠道细菌会引发什么问题,大多数人或许都认为有害肠道菌群会引发消化道问题,比如便秘、胃胀气或腹泻;但近日科学家们发现,有害细菌,或有益细菌水平不够或许和多发性硬化症发生直接相关,相关研究发表于Scientific Reports杂志上。
Ashutosh Mangalam博士表示,人类机体肠道中携带着数万亿个细菌,俗称为肠道微生物组,近年来多项研究表明,肠道菌群在改善并维持人体健康上扮演着重要作用。肠道细菌往往机体健康息息相关,为此研究人员就想知道是否肠道菌群和慢性自身免疫性疾病直接相关,比如多发性硬化症等,同时研究者还想知道是否自身免疫性疾病患者机体的肠道微生物组不同于健康个体的肠道微生物组。
研究者表示,实际上多发性硬化症患者有着和健康个体不同的肠道微生物组,尽管这是一项初步研究,但相关数据表明,多发性患者机体中有益菌群的水平较低,比如那些从健康食物(黄豆、亚麻)中获取效益的有益菌群。
【5】FAN:首次发现益生菌或可改善阿尔兹海默氏症患者大脑的认知功能!
doi:10.3389/fnagi.2016.00256
日前,一项刊登在国际杂志Frontiers in Aging Neuroscience上的研究报告中,来自伊斯兰阿萨德大学等机构的研究人员通过研究首次发现,益生菌能够改善人类大脑的认知功能,在最新的临床试验中,科学家们通过研究发现,在为期12周的研究中,每日单一剂量的乳酸菌和双歧杆菌或许能够明显改善在细微精神状态检查(MMSE)老年阿尔兹海默氏症患者的评分情况,MMSE是一种认知损伤的标准测试方法。
益生菌能够帮助机体抵御特定的感染性腹泻、肠激惹综合征、炎性肠病等疾病;长期以来研究者们假设,益生菌或许能够增强大脑认知功能,因为肠道菌群、胃肠道及大脑之间存在一种双向沟通的机制,即微生物群肠脑轴;在小鼠机体中,益生菌能够改善其学习和记忆能力,同时降低小鼠的焦虑感和抑郁表现,然而此前研究中研究者并未发现益生菌能够改善人类大脑的认知功能。
【6】Nat Commun:胃肠道细菌变化可阻止中风发生
doi: 10.1038/ncomms2266
来自瑞典查尔姆斯理工大学和哥德堡大学的研究人员证实人肠道菌群变化与表现出症状的动脉粥样硬化和中风相关联。这些研究发现于近期发表在Nature Communications期刊上。
人体含有的细菌细胞数量是人细胞的10倍多,其中大多数细菌细胞是在人肠道中发现的。除了我们的宿主基因组外,这些细菌含有大量的基因,它们一起被称作肠道宏基因组(gut metagenome)。
这种宏基因组如何影响我们的健康?当前已有很多研究人员正在设法解决这个问题。在之前的研究中,科学家们已发现几种疾病与肠道宏基因组的变化相关联。如今在一项新的研究中,研究人员也证实肠道宏基因组变化与动脉粥样硬化和中风相关联。
【8】Sci Rep:抗生素影响肠道菌群延缓阿尔茨海默病发展
DOI: 10.1038/srep30028
最近,芝加哥大学的研究人员发现广谱抗生素长期治疗能够使小鼠的淀粉样蛋白斑块减少,同时激活脑内的炎症性小胶质细胞。相关研究结果发表在国际学术期刊Scientific Reports上。
该研究还发现抗生素治疗后肠道菌群发生显著变化,这表明肠道菌群的组成和多样性可能通过调节免疫系统活性进而影响了阿尔茨海默病进展。
阿尔茨海默病有两个关键特征:其一是脑内淀粉样蛋白斑块的形成,其二是在中枢神经系统负责免疫系统功能的小胶质细胞出现炎症状态增加。淀粉样蛋白斑块的形成对阿尔茨海默病的发病起主要作用,而有研究认为神经炎症状态会影响阿尔茨海默病导致认知下降的速率。

【9】帕金森氏症患者肠道菌群特殊
doi:10.1002/mds.26069
根据赫尔辛基大学和赫尔辛基大学中心医院进行的一项研究发现,与健康对照者相比,帕金森氏症患者肠道有不同菌群。研究人员目前正在试图确定肠道微生物和帕金森氏症之间的联系。
我们最重要的发现是,帕金森病患者肠道中有比较少的普雷沃氏菌家族细菌,不同与对照组,帕金森病患者肠道几乎没有人有这个家族的大量细菌。这项研究发表在Movement Disorders杂志上。
研究人员尚未确定帕金森患者缺乏普雷沃氏菌科意味着什么,这些细菌是否可能保护他们的主人?还是缺乏普雷沃氏菌科只是患者肠功能紊乱病理的一部分? Sheperjans说:这是我们正试图回答的一个有趣问题。
【10】Neurology:重磅!首次发现细菌会直接影响阿尔兹海默氏症的疾病进展
doi:10.1212/WNL.0000000000003391
日前,一项刊登于国际杂志Neurology上的研究报告中,来自加州大学戴维斯分校神经和大脑研究所的研究人员通过研究首次发现,在晚发性(迟发性)的阿尔兹海默氏症患者大脑样本中存在较高水平的革兰氏阴性菌的抗原,相比对照而言,这些患者大脑样本中细菌脂多糖和大肠杆菌K99菌毛蛋白的水平较高,此外研究者还发现,这些脂多糖分子能够聚集在淀粉样斑块中,而这就和阿尔兹海默式症患者的病理学表现及疾病进展直接相关了。
研究者Xinhua Zhan说道,我们通过免疫组化方法对所有18个老化的大脑样本进行检测发现了革兰氏阴性菌的细胞组分:脂多糖和大肠杆菌K99菌毛蛋白,相对用蛋白印迹分析对照的结果而言,k99在阿尔兹海默式症患者的大脑中水平明显会增加,同时脂多糖还能够聚集在β淀粉样斑块上以及患者大脑的血管中。研究者并不确定是否细菌引发了阿尔兹海默式症还是该疾病导致的结果。
【11】微生物研究有助神经变性疾病疗法开发
数万亿的微生物栖息在人类的机体中,这些微生物群体被称之为微生物组,据估计这些微生物群体重2-6磅,其总体重是平均大脑体重的2倍,大部分的微生物生活在机体肠道中,其可以帮助机体消化食物,合成维生素以及抵御感染;但截止到现在研究者对微生物组的研究显示,微生物群体对机体的影响远远超过了肠道,其还会对人类大脑产生影响。
在过去10年里,有研究就表明肠道微生物组合一系列复杂的行为直接相关,比如情绪、情感、食欲等,然而肠道微生物组不仅可以可以帮助维持大脑的功能,而且可以影响个体患神经性障碍及心理障碍的风险,比如焦虑症、抑郁及自闭症等。研究者Christopher Lowry教授表示,当前最大的问题就是微生物组如何对机体大脑施加效应,而我们的研究可以揭示是否有益的微生物组可以被用来治疗或抑制压力相关的心理疾病,比如焦虑症和抑郁症等。
研究者表示,小鼠机体中的微生物组对压力比较敏感,而且压力诱导的小鼠母亲机体的微生物组的改变可以遗传给幼鼠,并且改变幼鼠的大脑发育。因此如果母亲机体的微生物生态系统因为感染、压力或饮食而发生改变的话,其新生儿肠道的微生物组就会发生改变而且会对后代医生有影响。
| 欢迎光临 中国病毒学论坛|我们一直在坚持! (http://bbs.virology.com.cn/) | Powered by Discuz! X3.2 |